Questões de Concurso Público IF-PR 2023 para Química
Foram encontradas 2 questões
Q2183169
Química
Ao se perguntar às pessoas de um grupo quais suas cores favoritas, a maioria responderá azul. Provavelmente, por
essa razão, a descoberta acidental do pigmento azul da Prússia por Diesbach no começo do séc. XVIII foi uma criação
tão preciosa. Do seu uso nas artes, atualmente esse material encontra aplicações em medicamentos até janelas
eletrocrômicas. O material é formado pela combinação de Fe(III) (Fe, Z = 26) e o íon ferrocianeto [Fe(CN)6]4-, em que Fe(II)
está em campo octaédrico coordenado ao ligante de campo forte CN-
. A cor azul intensa é proveniente de uma transição
de intervalência entre Fe(III) e o íon ferrocianeto. Ao oxidar eletroquimicamente o ferrocianeto ao ferricianeto [Fe(CN)6]3-
, a cor desaparece. Esse fenômeno é explorado nas janelas eletrocrômicas.
Ventura, D. O lendário azul da Prússia, cor que pode salvar ou tirar vidas. Disponível em www.bbc.com. Adaptado.
A distribuição eletrônica na valência do par associado à conversão eletroquímica de oxidação mencionada no texto é descrita por:
Ventura, D. O lendário azul da Prússia, cor que pode salvar ou tirar vidas. Disponível em www.bbc.com. Adaptado.
A distribuição eletrônica na valência do par associado à conversão eletroquímica de oxidação mencionada no texto é descrita por:
Q2183172
Química
Um vídeo que mostra dois homens da República Democrática do
Congo manuseando uma rocha de aparência metálica viralizou
recentemente nas redes sociais devido a comentários que atribuíram
à rocha misteriosa o mineral fictício vibranium do universo Marvel. No
vídeo, quando um homem conecta as extremidades de um fio a duas
regiões da rocha, uma lâmpada LED se acende, demonstrando uma
diferença de potencial e passagem de corrente elétrica. O que causa a
diferença de potencial ainda não foi esclarecido, mas se especula que
a rocha contenha minerais ricos em nióbio e cobalto, comumente
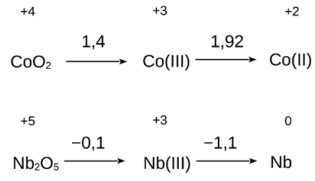
extraídos naquele país. Ao lado, são mostrados diagramas de Latimer
de espécies de cobalto e nióbio.
Admitindo-se que essas espécies possam estar participando do processo responsável pelo acendimento do LED, que opera entre 1,5 e 2,7 V, a possível pilha formada envolve:
Admitindo-se que essas espécies possam estar participando do processo responsável pelo acendimento do LED, que opera entre 1,5 e 2,7 V, a possível pilha formada envolve:
