Questões de Concurso Público EMGEPRON 2021 para Engenheiro Químico
Foram encontradas 47 questões
H2SO4+ CaCO3 → CaSO4 + H2O + CO2
Sabendo que cada caminhão é capaz de transportar até 7,1 toneladas de calcário e que o calcário tem 85% de CaCO3 , a quantidade aproximada de caminhões necessária para carregar o material neutralizante é: (Dados de P.M de S:32; Ca:40; C:12; O:16, H:1)
Na expressão 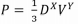 na qual P, D e V
representam pressão, densidade e velocidade,
respectivamente, os valores de X e Y, sendo a
expressão dimensionalmente correta, são os
seguintes:
na qual P, D e V
representam pressão, densidade e velocidade,
respectivamente, os valores de X e Y, sendo a
expressão dimensionalmente correta, são os
seguintes:
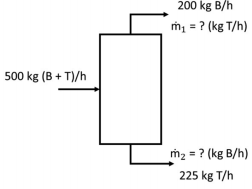
A vazão desconhecida (m1 e m2) dos componentes nas saídas do tanque, que pode ser calculada utilizando o balanço de massa sobre as espécies, é:
(Dados de P.M de Cu: 63,5; N:14; O:16; H:1 e constante de Faraday 96500 Cmol -1)