Questões de Concurso Público IF-RJ 2021 para Químico
Foram encontradas 6 questões
Q2012984
Química
Para expressar o potencial elétrico, na eletroquímica, foi
escolhido como referencial o eletrodo-padrão de:
Q2012985
Química
São características da Eletrólise:
I - Reação espontânea.
II - Dividida em Ígnea e Aquosa.
III - Precisa de energia elétrica para ocorrer.
Está correto o que se afirma em:
I - Reação espontânea.
II - Dividida em Ígnea e Aquosa.
III - Precisa de energia elétrica para ocorrer.
Está correto o que se afirma em:
Q2012987
Química
A Lei de Faraday aponta que a quantidade do produto
formado ou do reagente consumido por uma corrente elétrica é
estequiometricamente equivalente à quantidade de elétrons
fornecidos. O módulo da carga elétrica de um mol de elétrons
(_____________) é conhecido como Constante de Faraday e
simbolizado por F.
Assinale a alternativa que preenche, corretamente, a lacuna do texto:
Assinale a alternativa que preenche, corretamente, a lacuna do texto:
Q2012988
Química
À medida que uma reação prossegue, as concentrações dos
reagentes e produtos alteram-se e, numa célula eletroquímica,
a ddp (diferença de potencial ou força eletromotriz) torna-se
zero, quando a reação alcança o equilíbrio. O físico-alemão
Walther Hermann Nernst (1864- 1941) deduziu uma equação
que permite calcular a variação do potencial de uma pilha, em
determinado instante, a partir das concentrações em
quantidade de matéria das soluções dos eletrodos:
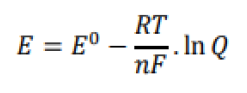
Considerando a equação, acima, E0 representa:
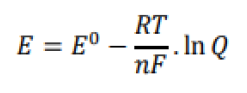
Considerando a equação, acima, E0 representa:
Q2013013
Química
A corrosão eletroquímica é a de maior presença, nos mais
diversos ambientes, é para tal processo corrosivo que se
prepara a superfície metálica das torres eólicas, com o objetivo
de impedir a formação de pilhas ou células corrosivas.
Caracteriza-se por:
I - Realizarem-se, necessariamente, na presença de água líquida.
II - Realizarem-se em temperaturas, acima do ponto de orvalho.
III - Realizarem-se devido à formação de pilhas de corrosão ou células eletroquímicas.
Está correto o que se afirma em:
I - Realizarem-se, necessariamente, na presença de água líquida.
II - Realizarem-se em temperaturas, acima do ponto de orvalho.
III - Realizarem-se devido à formação de pilhas de corrosão ou células eletroquímicas.
Está correto o que se afirma em: