Questões de Concurso Público SEED-PR 2022 para Área de Conhecimento: Química
Foram encontradas 40 questões
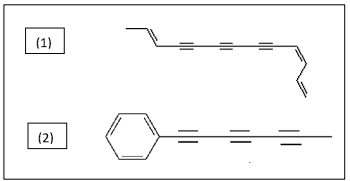
(Barbosa, 2011.)
O nome sistemático dos compostos 1 e 2 são, respectivamente:
( ) De acordo com a teoria de Bohr, o elétron do átomo de hidrogênio no estado fundamental pode absorver várias quantidades discretas de energia e, assim, elevar-se a um nível de energia mais alto. ( ) A teoria atômica de Dalton explicou as leis da combinação química propondo que a matéria consiste em átomos indestrutíveis com massas que não mudam no decorrer das reações químicas. ( ) Quando elétrons absorvem ou emitem energia ao passarem de uma órbita eletrônica para outra, a energia é dada pela equação: E = mZ2e 4 . h. ( ) Os raios catódicos são um fluxo de elétrons que se movem em linha reta e são dependentes do material dos eletrodos e do gás residual que existe no tubo.
A sequência está correta em
I. As interações dipolo-dipolo são mais fracas do que as forças entre íons e diminuem rapidamente com a distância, especialmente nas fases líquida e gás, em que as moléculas estão em rotação. II. O aumento do ponto de ebulição dos gases nobres, do hélio ao xenônio, se deve à energia das interações de London que diminui com o número de elétrons. III. As repulsões entre moléculas são o resultado da superposição de orbitais de moléculas vizinhas e do princípio da exclusão de Pauli.
Está correto o que se afirma em
I. Nos éteres, o oxigênio apresenta hibridação sp3 e o ângulo entre os grupos ligados ao oxigênio é de, aproximadamente, 110°. II. A solubilidade dos éteres em água diminui com o aumento do número de átomos de carbono. III. As temperaturas de ebulição dos éteres são mais altas que as dos alcanos de massa molar semelhante e bem mais baixa que as dos álcoois de mesma massa molar.
Está correto o que se afirma em