Questões de Concurso Público IF-MS 2019 para Química
Foram encontradas 25 questões
Q2047282
Química
No livro Desespero, de Stephen King, um dos
personagens faz a seguinte afirmação: “A gente tira o
cobre da terra com ácido sulfúrico. A melhor maneira
de aplicar é com esguichos... parecem grandes
molhadores de grama.”
Considerando que uma amostra de 2,0 kg, contendo 80% de óxido de cobre II, foi utilizada para reagir com o ácido citado no livro de Stephen King. Admitindo que os outros compostos da amostra não reagem com o ácido, determine a massa aproximada de ácido necessária para que todo o cobre da amostra sofra reação química.
Considere as seguintes massas molares em g.mol-1 : Cu = 63,5; O = 16; H = 1 e S = 32.
Considerando que uma amostra de 2,0 kg, contendo 80% de óxido de cobre II, foi utilizada para reagir com o ácido citado no livro de Stephen King. Admitindo que os outros compostos da amostra não reagem com o ácido, determine a massa aproximada de ácido necessária para que todo o cobre da amostra sofra reação química.
Considere as seguintes massas molares em g.mol-1 : Cu = 63,5; O = 16; H = 1 e S = 32.
Q2047283
Química
Segundo o Acordo de Paris, assinado por 195 países
em dezembro de 2015, os Estados adotarão, de
forma voluntária, medidas para reduzir as emissões
de gases-estufa a fim de limitar o aquecimento global
em 2 graus Celsius, mas com a meta mais ambiciosa
de 1,5 grau Celsius. Estima-se que, em 2002, a
concentração de dióxido de carbono na atmosfera
seja de aproximadamente 600 ppm (600×10-6 atm).
Sabendo que a constante de Henry, a 25ºC, para o
dióxido de carbono é aproximadamente 3,0×10-2
mol.L-1
.atm-1 e a constante de acidez para o ácido
carbônico é aproximadamente 5,0×10-7 mol.L-1
,
calcule qual o valor do pH da solução de CO2
dissolvido em água destilada equilibrada com a
atmosfera prevista para o ano 2020, considerando
que apenas o dióxido de carbono contribua para o pH
da solução.
Dados: log 2 = 0,30 e log 3 = 0,48
Dados: log 2 = 0,30 e log 3 = 0,48
Q2047284
Química
Titulações envolvem a adição de uma solução,
chamada titulante, colocada em uma bureta, a uma
solução que contém amostra, chamada de analito,
colocada em Erlenmeyer. Por exemplo, se um
químico ambiental estivesse estudando o escoamento
de resíduos de uma mina e precisasse conhecer a
concentração de ácido na água uma amostra de
efluentes da mina seria o analito e uma solução
básica de concentração conhecida seria o titulante.
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed 5, Bookman, 2011.)
Sobre titulação, assinale a alternativa correta:
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed 5, Bookman, 2011.)
Sobre titulação, assinale a alternativa correta:
Q2047285
Química
Considere uma reação hipotética com três reagentes (A, B e C) e um produto (D). A velocidade de formação de D
foi monitorada em quantidades diferentes dos reagentes, conforme a tabela abaixo:
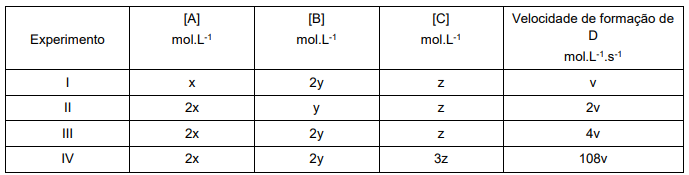
Determine a velocidade da reação em função de v se as concentrações de A, B e C, forem, respectivamente, igual a: 3x, 5y e 2z.

Determine a velocidade da reação em função de v se as concentrações de A, B e C, forem, respectivamente, igual a: 3x, 5y e 2z.
Q2047286
Química
A Teoria dos Orbitais Moleculares (TOM) é uma ferramenta útil na descrição de ligações químicas, na avaliação
da estabilidade química e na previsão de propriedades físicas das moléculas como absorção de luz e magnetismo.
Utilizando o conceito de ordem de ligação (OL) [OL = (EOL - EOAL) / 2 ], em que EOL é o número de elétrons em
orbitais ligantes e EOAL é o número de elétrons em orbitais antiligantes, é possível avaliar qualitativamente a
estabilidade de uma determinada molécula. Abaixo segue o diagrama de orbitais moleculares para o óxido nítrico
(NO), que no estado gasoso é uma molécula paramagnética.
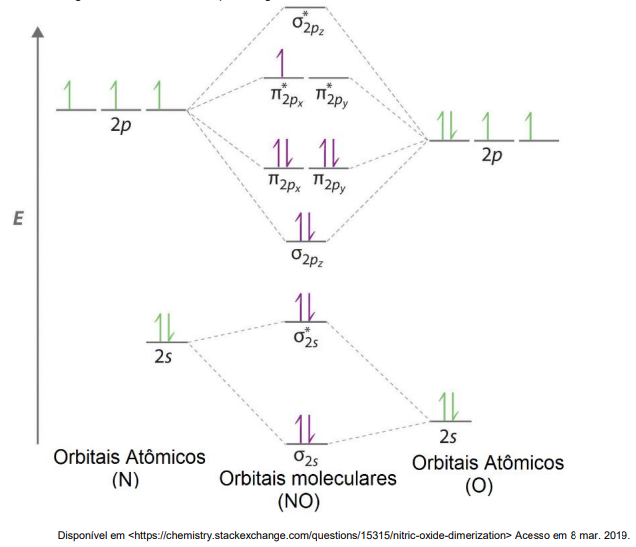
Sendo assim, escolha a alternativa que representa quais características serão apresentadas no íon NO+ .

Sendo assim, escolha a alternativa que representa quais características serão apresentadas no íon NO+ .