Questões de Concurso Público SES-DF 2018 para Médico - Cancerologia / Oncologia Clínica
Foram encontradas 15 questões
Ano: 2018
Banca:
IADES
Órgão:
SES-DF
Prova:
IADES - 2018 - SES-DF - Médico - Cancerologia / Oncologia Clínica |
Q1111188
Medicina
Paciente do sexo feminino, de 32 anos de idade, previamente
hígida, recém-diagnosticada com carcinoma ductal invasivo
em mama direita, com receptor de estrógeno negativo,
receptor de progesterona negativo, HER-2 escore 3 (FISH
positivo), Ki-67 = 50% e estadiamento T2 N0 M0, é
encaminhada pelo mastologista a uma consulta para discutir
proposta de terapia neoadjuvante. Ela refere que leu na
internet que a Food and Drug Administration (FDA) aprovou
recentemente uma nova medicação para câncer de mama, o
olaparibe.
Quanto à aprovação recente pelo FDA, em janeiro de 2018,
do uso de olaparibe em pacientes com câncer de mama,
assinale a alternativa correta.
Ano: 2018
Banca:
IADES
Órgão:
SES-DF
Prova:
IADES - 2018 - SES-DF - Médico - Cancerologia / Oncologia Clínica |
Q1111189
Medicina
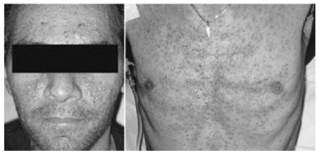
Paciente do sexo masculino, de 62 anos de idade, previamente hígido, com diagnóstico de adenocarcinoma de pulmão com mutação do EGFR, metastático para fígado, comparece à consulta ambulatorial pós-ciclo 1 de primeira linha de tratamento paliativo com gefitinibe. Refere aparecimento de lesões em tronco após o início do tratamento, sem outras queixas. Ao exame dermatológico, identifica-se rash eritematoso papulovesicular acneiforme pruriginoso em toda a extensão anterior e posterior do tronco, bem como em região malar grau 3 pelo CTCAE 4.0, como na imagem apresentada, claramente relacionadas ao tratamento com gefitinibe. Com relação ao caso descrito, assinale a alternativa correta.
Ano: 2018
Banca:
IADES
Órgão:
SES-DF
Prova:
IADES - 2018 - SES-DF - Médico - Cancerologia / Oncologia Clínica |
Q1111190
Medicina
Em março de 2017, a Food and Drug Administration (FDA)
aprovou, pela primeira vez, um tratamento oncológico para
carcinoma de células de Merkel metastático,
independentemente da exposição prévia ou não à
quimioterapia. Acerca desse tema, assinale a alternativa que
indica o medicamento recentemente aprovado em primeira
linha de tratamento paliativo para o tipo de neoplasia
mencionada.
Ano: 2018
Banca:
IADES
Órgão:
SES-DF
Prova:
IADES - 2018 - SES-DF - Médico - Cancerologia / Oncologia Clínica |
Q1111191
Medicina
Paciente do sexo feminino, de 59 anos de idade, previamente
hígida, recém-diagnosticada com carcinoma ductal invasivo
em mama direita, com receptor de estrógeno negativo, receptor
de progesterona negativo, HER-2 escore 1, Ki-67 = 30% e
estadiamento T3 N0 M0, está em programação de iniciar
tratamento neoadjuvante com AC-T (doxorrubicina 60 mg/m²
endovenoso D1 e ciclofosfamida 600 mg/m2
endovenoso D1 a
cada 21 dias por 4 ciclos, seguido de paclitaxel 80 mg/m2
endovenoso semanal por 12 semanas). A paciente questiona a
respeito de uma injeção que a prima dela havia utilizado
durante a quimioterapia para aumentar a imunidade.
Considerando o exposto e quanto ao uso de fator de
crescimento de colônias (filgrastim) como profilaxia primária
para redução do risco de neutropenia febril, segundo a
guideline da American Society of Clinical Oncology
(ASCO), é correto afirmar que a profilaxia primária
Ano: 2018
Banca:
IADES
Órgão:
SES-DF
Prova:
IADES - 2018 - SES-DF - Médico - Cancerologia / Oncologia Clínica |
Q1111192
Medicina
Considere paciente do sexo feminino, de 60 anos de idade,
previamente hígida, recém-diagnosticada com melanoma
cutâneo no braço esquerdo, cujo exame anatomopatológico da
ressecção evidenciou: melanoma maligno tipo nodular, CLARK
IV, Breslow = 4,2 mm, 38 mitoses por 10 campos de grande
aumento, infiltrado linfocitário leve, ulceração presente,
invasões angiolinfática e perineural ausentes, margens livres,
pT4b. Foram realizados pesquisa de linfonodo sentinela e
estadiamento sistêmico, sem evidência de doença.
Em abril de 2018, a Food and Drug Administration (FDA)
aprovou a combinação de dabrafenibe e trametinibe para uso
em tratamento adjuvante de melanoma. Com relação a essa
aprovação pela FDA, assinale a alternativa correta.