Questões de Concurso Público INB 2018 para Técnico em Química
Foram encontradas 3 questões
Ano: 2018
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
INB
Prova:
FUNDEP (Gestão de Concursos) - 2018 - INB - Técnico em Química |
Q1106227
Química
O urânio é um elemento químico muito cobiçado
economicamente devido ao seu poder bélico e à sua
aplicabilidade como combustível nas usinas nucleares.
Seu isótopo, o urânio-238, tende a sofrer decaimento,
liberando partículas e originando novas espécies.
Considere, hipoteticamente, que o urânio sofre
decaimentos radioativos conforme as equações
químicas a seguir.
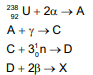
Nessas condições, é correto afirmar que o elemento X é a espécie:
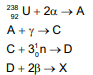
Nessas condições, é correto afirmar que o elemento X é a espécie:
Ano: 2018
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
INB
Prova:
FUNDEP (Gestão de Concursos) - 2018 - INB - Técnico em Química |
Q1106232
Química
Os químicos usam uma notação especial para especificar
a estrutura dos compartimentos dos eletrodos de células
galvânicas. Nessa notação, dois eletrodos, X e Y, de
uma pilha hipotética e suas respectivas soluções são
descritos a seguir.
X (s) / X2+ (1,05 mol/L) // Y2+ (1,10 mol/L) / Y (s)
Sobre a notação descrita, foram feitas as seguintes afirmações. I. As duas barras (//) indicam a ponte salina. II. X representa o eletrodo do anodo e Y, o eletrodo do catodo para reações espontâneas. III. O potencial da pilha se encontra em condição diferente do padrão.
Estão corretas as afirmações:
X (s) / X2+ (1,05 mol/L) // Y2+ (1,10 mol/L) / Y (s)
Sobre a notação descrita, foram feitas as seguintes afirmações. I. As duas barras (//) indicam a ponte salina. II. X representa o eletrodo do anodo e Y, o eletrodo do catodo para reações espontâneas. III. O potencial da pilha se encontra em condição diferente do padrão.
Estão corretas as afirmações:
Ano: 2018
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
INB
Prova:
FUNDEP (Gestão de Concursos) - 2018 - INB - Técnico em Química |
Q1106233
Química
O cloreto de hidrogênio (HCl (g)) é um gás muito utilizado
em diversas indústrias com muitas aplicabilidades, por
exemplo, para regenerar catalisadores nas indústrias
petroquímicas, como agente de limpeza, na produção de
metais duros, nas sínteses farmacêuticas, etc.
Considere as seguintes equações químicas e suas
respectivas entalpias de reações:
NH3 (g) + HCl (g) → NH4 Cl (s) ∆H0 = –176 kJ N2 (g) + 3H2 (g) → 2NH3 (g) ∆H0 = –92,2 kJ N2 (g) + 4H2 (g) + Cl2 (g) → 2NH4 Cl (s) ∆H0 = –628,9 kJ
Com base nas equações, é correto afirmar que a entalpia de reação de síntese do gás cloreto de hidrogênio é, em quilojoules, aproximadamente igual a:
NH3 (g) + HCl (g) → NH4 Cl (s) ∆H0 = –176 kJ N2 (g) + 3H2 (g) → 2NH3 (g) ∆H0 = –92,2 kJ N2 (g) + 4H2 (g) + Cl2 (g) → 2NH4 Cl (s) ∆H0 = –628,9 kJ
Com base nas equações, é correto afirmar que a entalpia de reação de síntese do gás cloreto de hidrogênio é, em quilojoules, aproximadamente igual a:
