Questões de Concurso Público IF-RS 2023 para Professor - Química
Foram encontradas 5 questões
Q2358152
Química
A capsaicina, princípio picante do fruto de várias espécies de pimenta (Capsicum e
Solanaceae), foi isolada em 1876, e sua estrutura foi determinada em 1919. A capsaicina tem
atividade anti-inflamatória e analgésica, por isso, pode ser utilizada para o tratamento de dores
causadas por doenças reumáticas. Em relação à molécula de capsaicina, analise as assertivas a seguir:
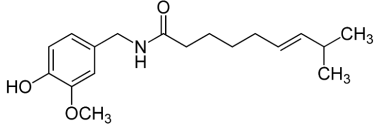
I. Apresenta as funções cetona e amina em sua estrutura.
II. Possui oito átomos de carbono com hibridização sp2 .
III. Apresenta dois carbonos terciários, oito carbonos secundários e dois carbonos primários.
IV. Possui três átomos de carbono com hibridização sp.
V. Apresenta fórmula molecular C18H27NO3.
Quais estão corretas?

I. Apresenta as funções cetona e amina em sua estrutura.
II. Possui oito átomos de carbono com hibridização sp2 .
III. Apresenta dois carbonos terciários, oito carbonos secundários e dois carbonos primários.
IV. Possui três átomos de carbono com hibridização sp.
V. Apresenta fórmula molecular C18H27NO3.
Quais estão corretas?
Q2358154
Química
Os átomos são os componentes básicos da matéria. Eles são as menores unidades
de um elemento que podem se combinar com outros elementos. Os modelos atômicos são
representações das ideias que se têm sobre a constituição da matéria. Considerando os modelos
atômicos propostos e os experimentos realizados para estudar a estrutura do átomo, analise as
assertivas a seguir e assinale V, se verdadeiras, ou F, se falsas.
( ) Em 1913, Bohr propôs um modelo no qual os elétrons orbitam o núcleo, porém com uma órbita definida e particular. Bohr conhecia os trabalhos de Planck e Einstein. Em seu modelo, os elétrons ocupam estados estacionários de energia fixa. Os elétrons podem realizar saltos quânticos de um estado de energia para outro em que é liberado um fóton.
( ) O físico inglês J. J. Thomson usou o tubo de raios catódicos e seu conhecimento da teoria eletromagnética para determinar a razão entre a carga elétrica e a massa de um elétron.
( ) O modelo atômico de Dalton propôs que a matéria é constituída de minúsculas partículas, como uma minúscula esfera maciça, impenetrável, indestrutível, indivisível e sem carga.
( ) Thomson propôs que um átomo podia ser imaginado como uma esfera com carga positiva uniforme de matéria, na qual os elétrons estão embutidos como passas em um bolo. Esse modelo chamado de “pudim de passas” foi a teoria aceita durante muitos anos.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
( ) Em 1913, Bohr propôs um modelo no qual os elétrons orbitam o núcleo, porém com uma órbita definida e particular. Bohr conhecia os trabalhos de Planck e Einstein. Em seu modelo, os elétrons ocupam estados estacionários de energia fixa. Os elétrons podem realizar saltos quânticos de um estado de energia para outro em que é liberado um fóton.
( ) O físico inglês J. J. Thomson usou o tubo de raios catódicos e seu conhecimento da teoria eletromagnética para determinar a razão entre a carga elétrica e a massa de um elétron.
( ) O modelo atômico de Dalton propôs que a matéria é constituída de minúsculas partículas, como uma minúscula esfera maciça, impenetrável, indestrutível, indivisível e sem carga.
( ) Thomson propôs que um átomo podia ser imaginado como uma esfera com carga positiva uniforme de matéria, na qual os elétrons estão embutidos como passas em um bolo. Esse modelo chamado de “pudim de passas” foi a teoria aceita durante muitos anos.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Q2358157
Química
Para a decomposição a 250 °C do pentacloreto de fósforo em tricloreto de fósforo e
cloro molecular, a constante de equilíbrio (Kp) é 1,05. Considerando o equilíbrio e que as pressões
parciais de PCl5 e PCl3 são 0,587 atm e 0,346 atm, respectivamente, assinale a alternativa que
apresenta a pressão parcial de Cl2 no equilíbrio a 250°C.
Q2358165
Química
A Tabela Periódica pode ser usada na predição de inúmeras propriedades, muitas das
quais são cruciais para a compreensão da Química. Em relação à classificação periódica dos elementos
e propriedades periódicas, assinale a alternativa INCORRETA.
Q2358167
Química
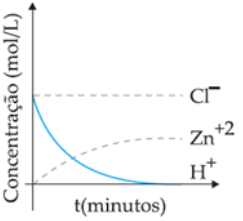
O gráfico a seguir representa a variação de concentração com o tempo durante a
reação de ácido clorídrico com zinco metálico. Analise-o e assinale a alternativa correta.