Na produção de óleo de soja, grãos de soja contendo 13,0% em massa de óleo e
87,0% de sólidos são moídos e vertidos em um tanque agitado (extrator), junto com uma corrente
reciclada de n-hexano líquido. A razão de alimentação é de 3 kg de hexano/kg de grãos moídos. Os
grãos moídos são suspensos no líquido, e praticamente todo o óleo nos grãos é extraído pelo hexano.
O efluente do extrator passa para um filtro. A torta de filtro contém 75,0% em massa de sólidos e o
resto é óleo e hexano, na mesma razão com que saem do extrator. A torta de filtro é descartada e o
filtrado líquido é vertido em um evaporador, no qual o hexano é vaporizado e o óleo permanece como
líquido. O óleo é armazenado em tambores e comercializado. O vapor de hexano é subsequentemente
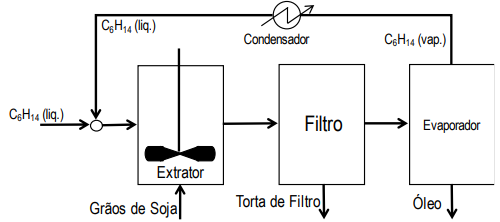
resfriado e condensado, e o hexano líquido é reciclado para o extrator. Um fluxograma e alguns dados
relevantes do processo são dados a seguir. Considerando esse processo, assinale a alternativa que
apresenta, respectivamente o rendimento de óleo de soja (kg óleo/kg grãos fornecidos), a alimentação
virgem de hexano requerida (kg C
6H
14/kg grãos fornecidos), e a razão do reciclo para a alimentação
virgem (kg hexano reciclado/kg alimentação virgem).