Questões de Concurso Público SEAD-AP 2022 para Papiloscopista, Edital nº 1
Foram encontradas 10 questões
Q1995925
Química
Texto associado
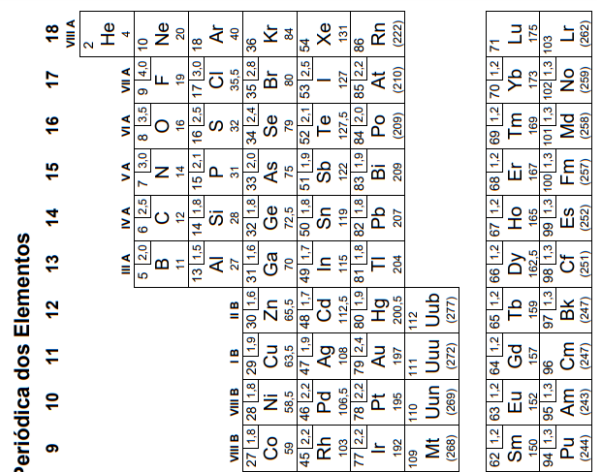
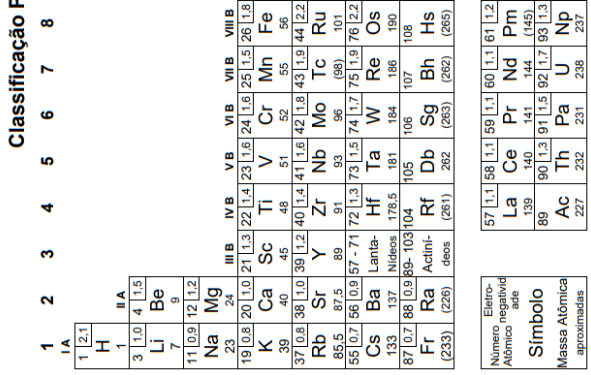
Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão específica de Química.


Na Química Forense uma série de testes podem ser usados para a
identificação de diferentes tipos de drogas. Um possível ensaio
para identificação de cocaína consiste na reação de uma amostra
dessa substância com uma solução recém-preparada de β-naftol
em hidróxido de sódio 40%. O desenvolvimento de uma cor azul
intensa indica resultado positivo.
A substância orgânica presente na solução utilizada nesse ensaio apresenta a seguinte estrutura
A substância orgânica presente na solução utilizada nesse ensaio apresenta a seguinte estrutura
Q1995926
Química
Texto associado


Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão específica de Química.


Em uma célula eletrolítica, a corrente elétrica é fornecida por uma
fonte externa e usada para promover uma reação química não-espontânea. Atualmente essa é uma das possíveis formas de
produção de hidrogênio gasoso a partir da eletrólise da água.
Considere esse processo eletrolítico ocorrendo segundo as
condições apresentadas na tabela a seguir:
Corrente Elétrica 10 A
Tempo 30 min
Pressão 1,0 atm
Temperatura 273 K
Sabendo que, nessas condições, foram recolhidos 1,7 L de gás hidrogênio é possível prever que o rendimento do processo foi, aproximadamente, de
(Dado: Constante de Faraday = 96.500 s.A.mol-1)
Corrente Elétrica 10 A
Tempo 30 min
Pressão 1,0 atm
Temperatura 273 K
Sabendo que, nessas condições, foram recolhidos 1,7 L de gás hidrogênio é possível prever que o rendimento do processo foi, aproximadamente, de
(Dado: Constante de Faraday = 96.500 s.A.mol-1)
Q1995927
Química
Texto associado


Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão específica de Química.


A composição de uma reação química em equilíbrio tende a mudar
quando as condições do sistema reacional são alteradas. Analise
as afirmações I, II e III a seguir.
I. A adição do catalisador óxido de vanádio V (V2O5) ao sistema em equilíbrio 2SO2(g) + O2(g) ⇌ 2SO3(g) promoverá aumento do rendimento do processo.
II. O aumento da pressão total sobre o sistema em equilíbrio Ni(s) + 4 CO(g) ⇌ Ni(CO)4(g) fará com que a concentração de monóxido de carbono diminua.
III. A diminuição da temperatura no sistema em equilíbrio CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g) (ΔH0 = +206 kJ) causará deslocamento da reação para o sentido direto.
Está correto o que se afirma em
I. A adição do catalisador óxido de vanádio V (V2O5) ao sistema em equilíbrio 2SO2(g) + O2(g) ⇌ 2SO3(g) promoverá aumento do rendimento do processo.
II. O aumento da pressão total sobre o sistema em equilíbrio Ni(s) + 4 CO(g) ⇌ Ni(CO)4(g) fará com que a concentração de monóxido de carbono diminua.
III. A diminuição da temperatura no sistema em equilíbrio CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g) (ΔH0 = +206 kJ) causará deslocamento da reação para o sentido direto.
Está correto o que se afirma em
Q1995928
Química
Texto associado


Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão específica de Química.


No ano de 2016 um novo sítio arqueológico foi descoberto no
Brasil, na zona rural de São Manuel (SP), e pode representar um
importante dado sobre a chegada dos humanos à América. Para
estimar a idade dos objetos encontrados, amostras de carvão que
estavam junto ao material foram enviadas para análise em
laboratório nos EUA, que procedeu a datação por radiocarbono.
Esse radioisótopo possui tempo de meia-vida de 5730 anos e, em
uma fonte de material recente, apresenta 18,2x103 desintegrações
em um período de 20 horas.
Considerando que a análise do material brasileiro enviado tenha apresentado 5,2x103 desintegrações para o mesmo período de tempo, é possível estimar que a idade da amostra analisada, em anos, é, aproximadamente, igual a
(Dado: log 3,5 = 0,54; log 2 = 0,30)
Considerando que a análise do material brasileiro enviado tenha apresentado 5,2x103 desintegrações para o mesmo período de tempo, é possível estimar que a idade da amostra analisada, em anos, é, aproximadamente, igual a
(Dado: log 3,5 = 0,54; log 2 = 0,30)
Q1995929
Química
Texto associado


Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão específica de Química.


O ácido nítrico (HNO3) é uma importante matéria-prima na
indústria química. Sua produção comercial ocorre através da
conversão da amônia (NH3) em uma sequência de três etapas
denominada Processo de Ostwald. Na primeira etapa, ocorre a
oxidação catalítica da amônia:
4NH3(g) + 5O2(g) → 4NO(g) + 6H2O(g)
Na segunda etapa, o óxido nítrico (NO) formado, quando exposto ao ar, se oxida rapidamente dando origem ao dióxido de nitrogênio (NO2):
2NO(g) + O2 → 2NO2(g)
Na terceira etapa, o NO2, quando dissolvido em água, forma o ácido nítrico como descrito na reação a seguir:
3NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
A quantidade máxima de ácido nítrico, em kg, que pode ser obtida a partir de 10.000 L de amônia é igual a
(Dado: volume molar = 25,0 L.mol-1)
4NH3(g) + 5O2(g) → 4NO(g) + 6H2O(g)
Na segunda etapa, o óxido nítrico (NO) formado, quando exposto ao ar, se oxida rapidamente dando origem ao dióxido de nitrogênio (NO2):
2NO(g) + O2 → 2NO2(g)
Na terceira etapa, o NO2, quando dissolvido em água, forma o ácido nítrico como descrito na reação a seguir:
3NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
A quantidade máxima de ácido nítrico, em kg, que pode ser obtida a partir de 10.000 L de amônia é igual a
(Dado: volume molar = 25,0 L.mol-1)