Questões de Concurso Público IFF 2018 para Professor - Química I
Foram encontradas 30 questões
O dióxido de carbono gerado em estações espaciais pode ser convertido em oxigênio pela reação com o superóxido de potássio, conforme a equação a seguir.
2CO2(g) + 4KO2(s) → 2K2CO3(s) + 3O2(g)
Tendo como referência a reação precedente, assinale a opção que apresenta a massa exata de KO2 necessária para a conversão total de 11,2 L de CO2 em oxigênio nas condições normais de temperatura e pressão (CNTP), considerando que o valor do volume molar de um gás ideal nas CNTP seja 22,4 L e que todos os gases comportem-se idealmente.
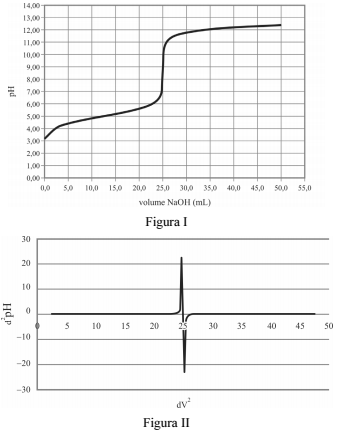
A figura I precedente mostra a variação do pH em função do volume de NaOH na titulação de 50,0 mL de uma solução de um ácido com uma solução de NaOH a 0,05 mol/L. A figura II mostra a segunda derivada da curva da figura I.
Considerando essas informações, assinale a opção correta a respeito
de volumetria e dos assuntos que esse tema suscita.
As soluções de íons cério (IV) e de íons permanganato são reagentes oxidantes fortes muito utilizados na titulação de amostras que contenham ferro. A tabela a seguir mostra as semirreações e os correspondentes potenciais padrão de eletrodo.

A partir das informações precedentes, assinale a opção correta a
respeito de eletroquímica e dos assuntos suscitados por esse tema.
A tabela a seguir lista as reações de combustão do carbono sólido C(s) como grafite, do gás hidrogênio H2(g) e do gás metano CH4(g). As variações de entalpia (ΔH) para essas reações também estão listadas na tabela.
reação ΔH
C(s) + O2(g) → CO2(g) x
H2(g) + ½O2(g) → H2O(l) y
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) z