Questões de Concurso Público Petrobras 2014 para Técnico(a) Químico(a) de Petróleo Junior
Foram encontradas 39 questões
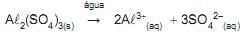
Um técnico pesou, em balança semianalítica, 17,1 g de Al2 (SO4 ) 3 , dissolveu o sal em água e levou o volume da solução a 500 mL em balão volumétrico.
As concentrações de Al3+ e SO42- , em mol/L, após a dissolução naquele volume final são, respectivamente,
A concentração de KIO3 na solução preparada em quantidade de matéria, em mol L-1 , é
Dado
M (KIO3 ) = 214 g mol -1
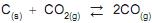
Para esse equilíbrio, a expressão da constante de equilíbrio Kc em função das concentrações das espécies, em quantidade de matéria, é:
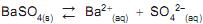
Sendo o seu produto de solubilidade a 25 o C igual a 1,0 x 10-10 , em solução saturada, a concentração de Ba 2+ , em mol/L, é

Um indicador do ponto final da titulação apropriado para uso nessa análise é o(a)