Questões de Concurso Público Transpetro 2011 para Químico de Petróleo Júnior
Foram encontradas 6 questões
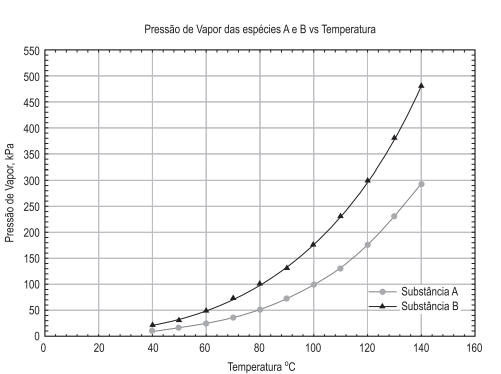
Uma mistura formada pelos componentes A e B se encontra à pressão de 120 kPa. No aquecimento dessa mistura, na pressão especificada, é formada a primeira bolha na temperatura de 100 °C. Dadas as respectivas curvas da pressão de vapor dos componentes A e B, presentes na figura acima, a composição aproximada da fase líquida e a da fase vapor em relação ao componente A, na temperatura de 100 °C, são, respectivamente,
A vazão mássica da corrente 3, em kg/h, é
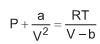 onde P, T e V são as condições de pressão, temperatura e volume molar do gás, respectivamente, R é a constante universal dos gases e a e b são constantes positivas características do gás. Nessas condições, o fator de compressibilidade do nitrogênio é
onde P, T e V são as condições de pressão, temperatura e volume molar do gás, respectivamente, R é a constante universal dos gases e a e b são constantes positivas características do gás. Nessas condições, o fator de compressibilidade do nitrogênio é
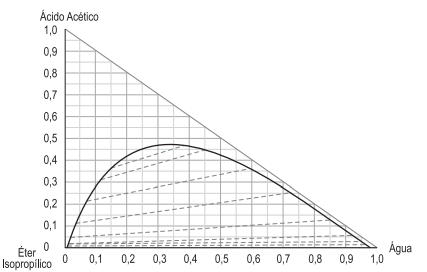
Considere que 1.000 kg/h de uma solução com 35% (massa) de ácido acético e 65% (massa) de água é alimentada a uma coluna de extração que opera em contracorrente. Para extrair o ácido acético, são usados 1.335 kg/h de éter isopropílico. É necessário que o produto rafinado contenha apenas 10% (massa) de ácido acético.
Utilizando o gráfico da figura acima, conclui-se que a composição mássica de éter isopropílico da corrente extrato é, aproximadamente,