Questões de Concurso Público PETROQUÍMICA SUAPE 2011 para Técnico de Laboratório Júnior
Foram encontradas 8 questões
Ano: 2011
Banca:
CESGRANRIO
Órgão:
PETROQUÍMICA SUAPE
Prova:
CESGRANRIO - 2011 - PETROQUÍMICA SUAPE - Técnico de Laboratório Júnior |
Q186499
Química
Texto associado
Uma solução é o resultado da dissolução de uma substância
(soluto) em outra denominada solvente.


Nas figuras acima, o solvente é a água e o soluto é o sulfato de cobre penta-hidratado, de fórmula CuSO4 .5H2O. Massa igual a 0,5 g do soluto foi dissolvida em água e o volume final da solução ajustado para 100 mL. A concentração aproximada da solução resultante, em mol/L, é
Ano: 2011
Banca:
CESGRANRIO
Órgão:
PETROQUÍMICA SUAPE
Prova:
CESGRANRIO - 2011 - PETROQUÍMICA SUAPE - Técnico de Laboratório Júnior |
Q186500
Química
Hidróxido de sódio é um eletrólito forte que, em meio aquoso, se dissocia totalmente em Na+ e OH - . A 100 mL de solução aquosa de NaOH 0,1 mol/L, acrescenta-se água destilada para ajustar volume a 1,0 L. Após diluição da solução original de hidróxido de sódio, o pH da solução resultante será igual a
Ano: 2011
Banca:
CESGRANRIO
Órgão:
PETROQUÍMICA SUAPE
Prova:
CESGRANRIO - 2011 - PETROQUÍMICA SUAPE - Técnico de Laboratório Júnior |
Q186501
Química
O esquema acima representa os procedimentos práticos para promover a reação entre soluções aquosas de ácido clorídrico (no frasco Erlenmeyer) e hidróxido de sódio (na bureta), utilizando um indicador para acusar o ponto final da seguinte reação:

Se, no frasco Erlenmeyer, há 25,00 mL de HCL(aq) 0,200 mol/L, o volume de NaOH(aq) 0,100 mol/L que deve escoar da bureta, em mL, até se atingir o ponto estequiométrico, é

Se, no frasco Erlenmeyer, há 25,00 mL de HCL(aq) 0,200 mol/L, o volume de NaOH(aq) 0,100 mol/L que deve escoar da bureta, em mL, até se atingir o ponto estequiométrico, é
Ano: 2011
Banca:
CESGRANRIO
Órgão:
PETROQUÍMICA SUAPE
Prova:
CESGRANRIO - 2011 - PETROQUÍMICA SUAPE - Técnico de Laboratório Júnior |
Q186505
Química
O ácido clorídrico é um eletrólito forte que se ioniza por completo em água, conforme a equação simplificada abaixo.
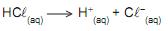
O volume, em mL, de solução aquosa de HCL0,1 mol/L necessário para o preparo de 1 L de solução com pH = 3 é
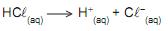
O volume, em mL, de solução aquosa de HCL0,1 mol/L necessário para o preparo de 1 L de solução com pH = 3 é
Ano: 2011
Banca:
CESGRANRIO
Órgão:
PETROQUÍMICA SUAPE
Prova:
CESGRANRIO - 2011 - PETROQUÍMICA SUAPE - Técnico de Laboratório Júnior |
Q186506
Química
A análise gravimétrica de um sal hidratado, visando a determinar o número de moléculas de água de hidratação, baseia-se nas seguintes etapas: leve aquecimento em estufa para eliminar umidade, resfriamento em dessecador, pesagem da amostra, forte aquecimento para eliminar a água de hidratação e resfriamento em dessecador seguido de pesagem da amostra, agora sem a água de hidratação.
Na etapa anterior ao forte aquecimento, pesou-se um sulfa- to ferroso hidratado (amostra), e a massa medida foi igual a 2,010 g. Após forte aquecimento em mufla, pesou-se o sulfato ferroso, sem a água de hidratação, e a massa medida foi igual a 1,095 g. De posse desses dados obtidos, conclui-se que o sal hidratado tem fórmula
Na etapa anterior ao forte aquecimento, pesou-se um sulfa- to ferroso hidratado (amostra), e a massa medida foi igual a 2,010 g. Após forte aquecimento em mufla, pesou-se o sulfato ferroso, sem a água de hidratação, e a massa medida foi igual a 1,095 g. De posse desses dados obtidos, conclui-se que o sal hidratado tem fórmula
