Questões de Química - Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador para Concurso
Foram encontradas 123 questões
H2O2(aq) → H2O (l) + 0,5 O2 (g)
A Tabela abaixo foi construída a partir de dados experimentais e mostra a variação da concentração do peróxido de hidrogênio que vai se decompondo em função do tempo.
[H2O2] mol/L Tempo (min) 1,2 0 1 15 0,6 25 0,4 30 0,2 45 0,1 60
Tabela2. Dados experimentais da decomposição do peróxido de hidrogênio, à 1atm.
Diante do exposto, assinale a alternativa correta utilizando os dados acima.
NO(g) + O3(g) → NO2(g) + O2(g)
Dados cinéticos dessa reação obtidos a T = 298 K foram medidos por técnica de fluxo rápido; alguns desses dados constam no quadro a seguir.

A lei da velocidade para a reação mencionada é:
No que se refere às escalas de temperatura, julgue o item subsequente.
A temperatura pode ser determinada por uma escala
padronizada, equivalente ao conceito de energia do
movimento molecular. O zero absoluto é uma temperatura
em que o movimento das moléculas cessa, sendo esse valor,
na escala absoluta, ou escala Kelvin, igual a −273 K. Na
escala Kelvin, a temperatura absoluta é inversamente
proporcional à energia cinética média de translação das
moléculas de um gás.
Com base nessas informações, julgue o próximo item.
Se a taxa de produção de oxigênio (d[O2]/dt) for igual a
3,0 × 10−5 mol/s, a taxa de consumo de ozônio (d[O3]/dt)
será igual a −2,0 × 10−5 mol/s.
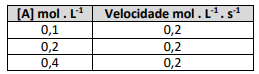
A partir das informações, a Lei de Velocidade para esta reação será de: