Questões de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro. para Concurso
Foram encontradas 87 questões
Julgue o item seguinte, referentes ao estudo dos gases.
Os gases diferem de líquidos e sólidos, pois o volume de
uma amostra de gás depende fortemente de sua temperatura e
da pressão que lhe é aplicada. Experimentalmente,
descobriu-se que todos os gases comuns se comportam
aproximadamente da mesma maneira, sendo esse
comportamento descrito pelas leis dos gases. Assim, para
quase todos os gases, o volume de uma amostra de gás a
temperatura constante é inversamente proporcional à
pressão.
Julgue o item seguinte, referentes ao estudo dos gases.
A investigação da relação entre o volume e a temperatura de
um gás mostra que gases sofrem contração quando sujeitos a
um aumento significativo de temperatura. Quando a pressão
e a quantidade de matéria de um gás são mantidas
constantes, o volume desse gás é inversamente proporcional
à temperatura.
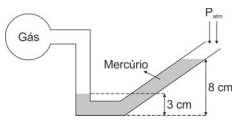
Sabendo que a pressão atmosférica local é de 76 cmHg, a pressão do gás é
I - A temperatura de equilíbrio será 50 ºC.
II - A água fria sofre aumento de energia interna e de entropia.
III - A água fria sofre aumento de entalpia e diminuição de entropia.
IV - A água quente sofre diminuição de energia interna e aumento de entropia.
Quais estão corretas?