Questões de Química - Fórmulas, Balanceamento e Leis ponderais das reações químicas para Concurso
Foram encontradas 123 questões
2Mg + O2 → 2MgO
Com essa reação foram realizados dois experimentos cujos dados constam nesta tabela:
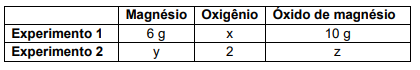
Utilizando as leis ponderais, é correto afirmar que os valores de x, y e z, em gramas, que completam, correta e respectivamente, a tabela são
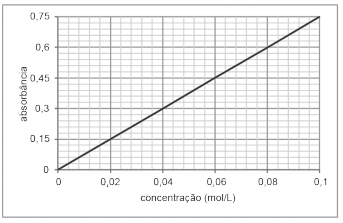
Uma amostra correspondendo a uma solução aquosa contendo Cu+2 passou pelo seguinte procedimento: uma alíquota de 10 mL dessa amostra foi completamente diluída em água até atingir um volume final de solução de 50 mL; uma alíquota dessa solução foi analisada no espectrômetro obtendo-se uma absorbância igual a 0,45.
A concentração de Cu+2 na amostra inicial, em mol L-1 , é
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
Etapa 1: 2 NO(g)
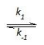 N2O2(g) (rápida, equilíbrio)
N2O2(g) (rápida, equilíbrio) Etapa 2: N2O2(g) + Br2(g)
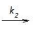 2NOBr (lenta)
2NOBr (lenta) A constante de velocidade para a reação entre óxido nítrico e bromo pode ser expresso em função das constantes k1, k-1 e k2 por meio da expressão:
A fórmula molecular da referida substância orgânica é