Questões de Concurso Militar EsPCEx 2011 para Cadete do Exército - 3° Dia
Foram encontradas 5 questões
4 C3H5(NO3)3(l) → 6 N2(g) + 12 CO(g) + 10 H2O(g) + 7 O2(g)
Considerando os gases acima como ideais, a temperatura de 300 Kelvin (K) e a pressão de 1 atm, o volume gasoso total que será produzido na detonação completa de 454 g de C3H5(NO3)3(l) é:
Dados:
Elemento H(hidrogênio) C( carbono) O ( Oxigênio) N( nitrogênio)
Massa 1 12 16 14
atômica(u)
Constante universal dos gases: R=8,2 · 10-2 atm · L · K-1 · mol-1
A concentração em mol · L-1 dos íons sulfato ( SO
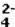 ) presentes na solução final é :
) presentes na solução final é :
Um laboratorista pesou separadamente uma amostra I, de hidróxido de sódio (NaOH), e uma amostra II, de óxido de cálcio (CaO), e, como não dispunha de etiquetas, anotou somente a soma das massas das amostras (I + II) igual a 11,2 g.
Cada uma das amostras I e II foi tratada separadamente com ácido sulfúrico (H 2SO4) produzindo, respectivamente, sulfato de sódio (Na2SO4) mais água (H2O) e sulfato de cálcio (CaSO4) mais água (H2O). Considere o rendimento das reações em questão igual a 100%.
Sendo a soma das massas dos sais produzidos (Na 2SO4 + CaSO4) igual a 25,37 g, então a massa da amostra I de hidróxido de sódio (NaOH) e a massa de amostra II de óxido de cálcio (CaO) são, respectivamente:
Dados:

A composição química do cimento Portland, utilizado na construção civil, varia ligeiramente conforme o que está indicado na tabela abaixo:
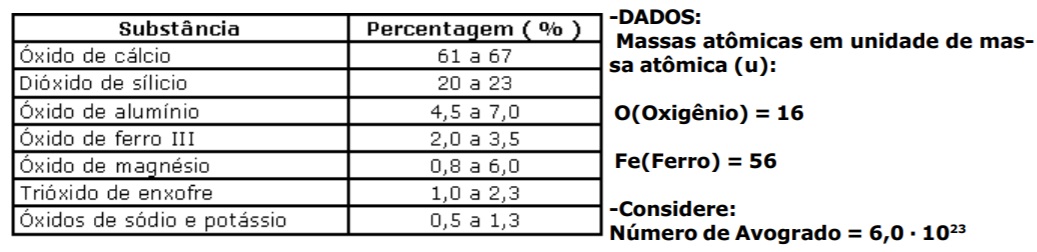
Assinale a alternativa correta:
Em uma eletrólise ígnea do cloreto de sódio, uma corrente elétrica, de intensidade igual a 5 ampères, atravessa uma cuba eletrolítica, com o auxilio de dois eletrodos inertes, durante 1930 segundos.
O volume do gás cloro, em litros, medido nas CNTP, e a massa de sódio, em gramas, obtidos nessa eletrólise, são, respectivamente: