Questões de Concurso Público MPE-SP 2016 para Analista Técnico Científico - Engenheiro Químico
Foram encontradas 3 questões
Ano: 2016
Banca:
VUNESP
Órgão:
MPE-SP
Prova:
VUNESP - 2016 - MPE-SP - Analista Técnico Científico - Engenheiro Químico |
Q792996
Química
“Consideram-se agentes químicos as substâncias, compostos
ou produtos que possam penetrar no organismo
pela via respiratória, nas formas de poeiras, fumos,
névoas, neblinas, gases ou vapores, ou que, pela natureza
da atividade de exposição, possam ter contato ou
ser absorvidos pelo organismo através da pele ou por
ingestão.”
Diante do exposto, pode-se afirmar corretamente que
Diante do exposto, pode-se afirmar corretamente que
Ano: 2016
Banca:
VUNESP
Órgão:
MPE-SP
Prova:
VUNESP - 2016 - MPE-SP - Analista Técnico Científico - Engenheiro Químico |
Q793004
Química
Dentre os gases do efeito estufa que estão aumentando
de concentração, podem ser citados o dióxido de carbono
e o metano. Sabe-se que a quantidade de metano
emitida é bem menor, mas seu potencial de aquecimento
é cerca de 21 vezes superior ao do dióxido de carbono.
Nesse sentido, um pesquisador sugeriu que o metano
fosse queimado como forma de atuar no problema. Com
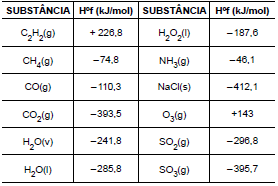
base nos dados de calores de formação a 25 ºC, assinale
a alternativa que indica corretamente o calor de reação
da combustão do metano em kJ/mol.

Ano: 2016
Banca:
VUNESP
Órgão:
MPE-SP
Prova:
VUNESP - 2016 - MPE-SP - Analista Técnico Científico - Engenheiro Químico |
Q793006
Química
Para a reação de produção de amônia, tem-se:
1 N2 (g) + 3 H2 (g) → 2 NH3 (g)
Dados: Massa Molar (N2 ) = 28 kg/kmol; Massa Molar (H2 ) = 2 kg/kmol. A vazão mássica de N2 na alimentação para produção de 1700 kg/dia de amônia é
1 N2 (g) + 3 H2 (g) → 2 NH3 (g)
Dados: Massa Molar (N2 ) = 28 kg/kmol; Massa Molar (H2 ) = 2 kg/kmol. A vazão mássica de N2 na alimentação para produção de 1700 kg/dia de amônia é