Questões de Concurso Público SEAP-DF 2013 para Professor - Química
Foram encontradas 5 questões
Q398907
Química
Considere as espécies químicas:
SF4 [ SiCl4]2- IF5 [ BCI4 ] -
( I ) ( II ) ( III ) ( IV )
As espécies cujos átomos em negrito utilizam um conjunto de orbitais híbridos sp3d. ao estabelecerem ligações químicas, são:
Dados: B (Z = 5 ) ; F (Z = 9 ) ; Si (Z = 14) ; S (Z = 16 ) ; Cl (Z = 17 ).
SF4 [ SiCl4]2- IF5 [ BCI4 ] -
( I ) ( II ) ( III ) ( IV )
As espécies cujos átomos em negrito utilizam um conjunto de orbitais híbridos sp3d. ao estabelecerem ligações químicas, são:
Dados: B (Z = 5 ) ; F (Z = 9 ) ; Si (Z = 14) ; S (Z = 16 ) ; Cl (Z = 17 ).
Q398908
Química
0 gráfico abaixo mostra a variação das primeiras energias de ionização ( I ) dos elementos químicos em função do aumento do número atômico.
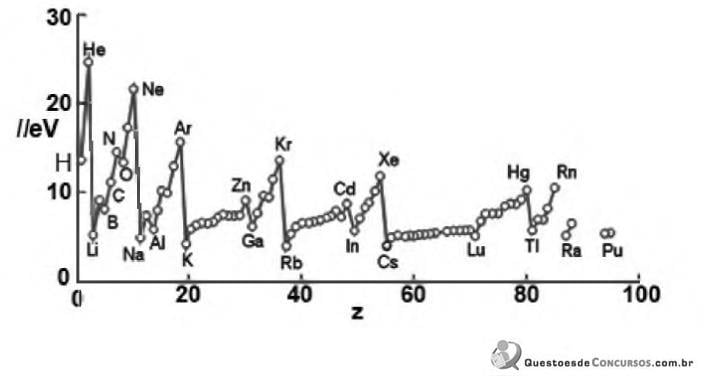
Analisando o gráfico podemos afirmar que:

Analisando o gráfico podemos afirmar que:
Q398909
Química
O desenvolvimento do modelo atômico foi realizado com a inestimável colaboração de diversos cientistas, através de experimentos clássicos, tais como:
• Experimento de John Joseph Thomson (1897) (A)
• Experimento com tubo de raios canais Eugen Goldstein (1886) (B)
• Experimento de William Crookes (1858) (C)
• Experimento de Robert Andrews Millikan (1908) (D)
Assinale a alternativa que apresenta a conclusão de cada um dos experimentos (A, B, C, e D)
• Experimento de John Joseph Thomson (1897) (A)
• Experimento com tubo de raios canais Eugen Goldstein (1886) (B)
• Experimento de William Crookes (1858) (C)
• Experimento de Robert Andrews Millikan (1908) (D)
Assinale a alternativa que apresenta a conclusão de cada um dos experimentos (A, B, C, e D)
Q398916
Química
O íon S032- é de grande importância na química ambiental no problema da chuva ácida. Esse íon é também usado como conservante em alguns alimentos. Para a padronização de uma solução da Na2S03 preparada pela dissolução de certa quantidade desse sal em 1 litro de água adotou-se o seguinte procedimento: em um erlenmeyer de 500 mL imerso em gelo adicionou-se 25,00 mL de NalO3 0,01299 M, 25 ml de água e 10 mL de H2S041,0 M e 25,00 mL da solução de sulfito de sódio (reação 1). A seguir, adicionou-se 2,0 g de Kl sólido (reação 2). O l2 formado foi titulado com solução padrão de tiossulfato de sódio 0,1017 M e o volume utilizado foi de 16,45 mL (reação 3). Calcular a concentração da solução de Na2S03. Considere a seqüência de reações (equacões não balanceadas) abaixo:
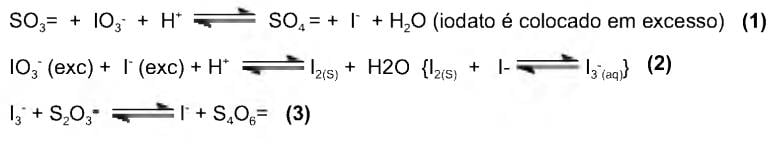
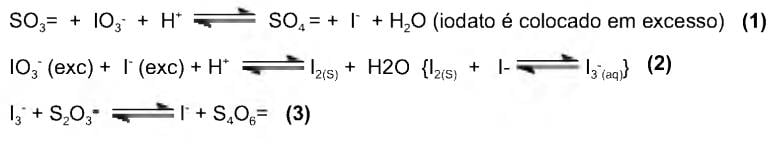
Q398921
Química
Calcule a massa molar do gás nobre criptônio, Kr, em uma amostra natural que consiste de: 0,3% de 78Kr (massa nuclídica de 77,92 g mol-1), 2,3% de 80Kr (massa nuclídica de 79,91 g mol-1), 11,6% de 82Kr (massa nuclídica de 81,91 g mol-1 ), 11,5% de 83Kr (massa nuclídica de 82,92 g mol-1), 56,9% de 84Kr (massa nuclídica de 83,91 g mol-1) e __________ de 86Kr (massa nuclídica de 85,91 g mol-1 ).
Assinale a alternativa que complete corretamente a lacuna.
Assinale a alternativa que complete corretamente a lacuna.