Questões de Concurso Público SEDUC-PE 2016 para Professor de Química
Foram encontradas 5 questões
Q701266
Química
Para quantificar sulfato em uma amostra adequadamente
preparada foi elaborada uma curva de calibração a partir da
diluição de uma solução padrão com concentração 100,0 mg.L-1
.
A curva de calibração utilizou as seguintes soluções:
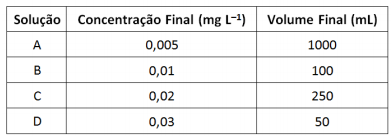
Sobre as soluções preparadas são feitas as afirmativas a seguir. I. Para preparar as soluções A e C foram utilizados os mesmos volumes da solução padrão. II. Para preparar a solução B foi utilizado o menor volume da solução padrão. III. Para preparar a solução D foi utilizado o maior volume da solução padrão. Está correto o que se afirma em

Sobre as soluções preparadas são feitas as afirmativas a seguir. I. Para preparar as soluções A e C foram utilizados os mesmos volumes da solução padrão. II. Para preparar a solução B foi utilizado o menor volume da solução padrão. III. Para preparar a solução D foi utilizado o maior volume da solução padrão. Está correto o que se afirma em
Q701268
Química
Um técnico preparou em um balão volumétrico 250 mL de uma
solução diluída de ácido clorídrico (a 20ºC), pipetando
adequadamente 8,4 mL do ácido concentrado 37% m/m de
densidade 1,19 g.cm-3
(a 20ºC).
A concentração da solução preparada, em mol.L-1
é de,
aproximadamente,
Dados: Massas molares: H = 1g.mol-1
Cl = 35,5 g.mol–1
Q701272
Química
Na determinação do teor de acidez de uma amostra de suco de
laranja comercial, 10,00 mL de amostra foram levados para
erlenmeyer. Adicionou-se água destilada até completar cerca de
50 mL, 3 gotas de fenolftaleína e titulou-se contra solução padrão
de NaOH até mudança de coloração. Na titulação, foram gastos
3,90 mL de solução padrão 0,100 mol.L–1
.
A acidez é expressa em termos do teor (porcentagem
massa/volume) de ácido cítrico, cuja fórmula estrutural é
apresentada a seguir.
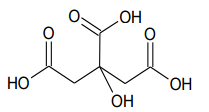
Assinale a opção que expressa a acidez da amostra. Dados. Massa molar. Ácido Cítrico: 192 g.mol –1 .

Assinale a opção que expressa a acidez da amostra. Dados. Massa molar. Ácido Cítrico: 192 g.mol –1 .
Q701275
Química
A análise da concentração de ortofosfato em corpos d’água pode
ser feita utilizando o método colorimétrico. Nesse método,
o reagente combinado contendo K(SbO)C4H4O6
, (NH4
)6Mo7O24 e
ácido ascórbico reage em meio ácido com o ortofosfato,
produzindo uma cor azul, cuja intensidade é determinada no
espectrofotômetro.
No preparo de 100 mL do reagente combinado utiliza-se 5 mL de
uma solução de K(SbO)C4H4O6 3,5 g.L-1
e 15 mL de uma solução
de (NH4
)6Mo7O24 40 g.L-1
.
Nessa solução do reagente combinado as concentrações
aproximadas (em g.L-1
) de K(SbO)C4H4O6 e de (NH4
)6Mo7O24 são,
respectivamente,
Q701278
Química
O ácido benzoico foi descoberto no século XVI e recebeu esse
nome por ter sido extraído do benjoeiro.
Em 1875, Salkowski verificou que esse ácido atua como fungicida
e, desde então, o ácido benzoico vem sendo usado como
germicida na preservação de alimentos e como adjuvante
farmacológico anti-fúngico, normalmente em concentrações que
variam entre 0,05 a 0,15%. Trata-se de um composto de fórmula
molecular C7H6O2
(massa molar = 122 g.mol -1
) pouco solúvel em
água.
Em uma solução aquosa, comporta-se como um ácido fraco, com
pKa = 4.
Uma solução aquosa de ácido benzoico em concentração 0,12%
(m/v) apresenta pH aproximadamente igual a