Questões de Concurso Público Colégio Pedro II 2018 para Professor - Química
Foram encontradas 25 questões
Ano: 2018
Banca:
Colégio Pedro II
Órgão:
Colégio Pedro II
Prova:
Colégio Pedro II - 2018 - Colégio Pedro II - Professor - Química |
Q946153
Química
O ácido nítrico é muito utilizado pela indústria química, principalmente em processos de nitrificação
de compostos orgânicos, na fabricação de vernizes, fertilizantes agrícolas, celuloses, salitre (nitrato
de potássio), pólvora negra, trinitrotolueno (TNT), nitroglicerina, seda artificial, ácido benzoico, fibras
sintéticas, galvanoplastia, ácido pícrico, nylon, entre outros. A produção industrial de ácido nítrico
se dá pelo Processo Ostwald, que envolve as seguintes reações químicas:
4 NH3(g) + 5 O2(g) → 4 NO(g) + 6 H2O(g) 2 NO(g) + O2(g) → 2 NO2(g) 3 NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
Supondo-se que o rendimento esperado nesse processo seja de 90% e que a amônia utilizada apresente 20% de impurezas, a massa de amônia, em toneladas, necessária para obtenção de 6,3 t de ácido nítrico será de, aproximadamente:
4 NH3(g) + 5 O2(g) → 4 NO(g) + 6 H2O(g) 2 NO(g) + O2(g) → 2 NO2(g) 3 NO2(g) + H2O(l) → 2HNO3(aq) + NO(g)
Supondo-se que o rendimento esperado nesse processo seja de 90% e que a amônia utilizada apresente 20% de impurezas, a massa de amônia, em toneladas, necessária para obtenção de 6,3 t de ácido nítrico será de, aproximadamente:
Ano: 2018
Banca:
Colégio Pedro II
Órgão:
Colégio Pedro II
Prova:
Colégio Pedro II - 2018 - Colégio Pedro II - Professor - Química |
Q946154
Química
O gás cloreto de carbonila (COCl2) é usado na síntese de muitos compostos orgânicos e pode ser
obtido a partir da reação entre monóxido de carbono e gás cloro. Observe a tabela a seguir que
demonstra as concentrações dos reagentes, em mol.L-1
, e a velocidade da reação, em mol de
produto.L-1
.s-1
, obtidas através de experimentos feitos a uma determinada temperatura:
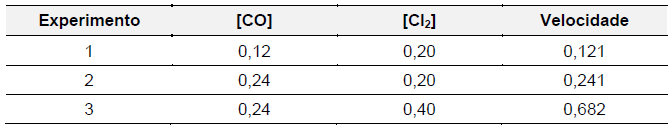
Dado que log 2,8 = 0,45 e log 2 = 0,3, o valor da constante da velocidade desta reação é

Dado que log 2,8 = 0,45 e log 2 = 0,3, o valor da constante da velocidade desta reação é
Ano: 2018
Banca:
Colégio Pedro II
Órgão:
Colégio Pedro II
Prova:
Colégio Pedro II - 2018 - Colégio Pedro II - Professor - Química |
Q946155
Química
Um aluno encontrou sobre a bancada do laboratório de Química quatro frascos numerados de I a
IV, contendo líquidos incolores. Sua professora lhe entregou 4 etiquetas com fórmulas moleculares
(CH2O, C2H6O, C3H6O e C4H10O) e a tabela abaixo para que ele pudesse identificar cada frasco
com o correspondente nome do composto em seu interior.
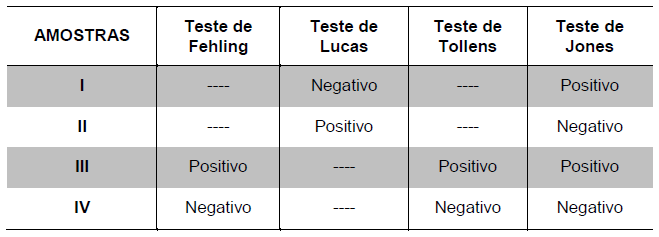
O aluno concluiu que as amostras contidas nos frascos I, II, III e IV eram, respectivamente,

O aluno concluiu que as amostras contidas nos frascos I, II, III e IV eram, respectivamente,
Ano: 2018
Banca:
Colégio Pedro II
Órgão:
Colégio Pedro II
Prova:
Colégio Pedro II - 2018 - Colégio Pedro II - Professor - Química |
Q946156
Química
A tabela a seguir evidencia os valores de ∆H de combustão, em kJ.mol-1
, de algumas substâncias
que podem ser usadas como combustíveis:
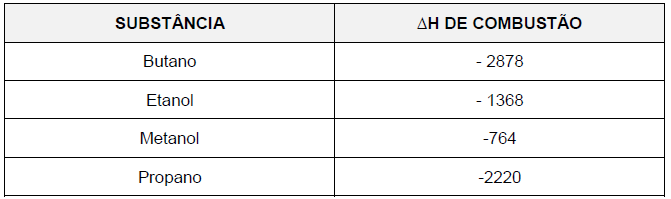
O combustível que lança na atmosfera a maior quantidade de gás poluente, para uma mesma quantidade de energia produzida, é

O combustível que lança na atmosfera a maior quantidade de gás poluente, para uma mesma quantidade de energia produzida, é
Ano: 2018
Banca:
Colégio Pedro II
Órgão:
Colégio Pedro II
Prova:
Colégio Pedro II - 2018 - Colégio Pedro II - Professor - Química |
Q946157
Química
O metanol líquido pode ser obtido a partir da reação de síntese entre monóxido de carbono e gás
hidrogênio. As entalpias de formação das substâncias citadas são, respectivamente, -238,4 kJ.mol1
e -110,5 kJ.mol-1
.
O valor da variação de entropia da vizinhança desse sistema a 25°C, em J.K-1 , é:
O valor da variação de entropia da vizinhança desse sistema a 25°C, em J.K-1 , é: