Questões de Concurso Público Transpetro 2011 para Técnico Químico
Foram encontradas 2 questões
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2011 - Transpetro - Técnico Químico |
Q170991
Química
Em solução aquosa, há reações em que a união de íons positivos a íons negativos conduzem à formação de substâncias muito pouco solúveis. Isso acontece, por exemplo, quando solução aquosa de nitrato de chumbo II entra em contato com solução aquosa de cromato de potássio. Íons chumbo se unem instantaneamente a íons cromato formando cromato de chumbo II com valor de 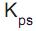 = 1,8 x 10-14 .
= 1,8 x 10-14 .
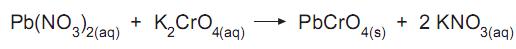
Se a uma solução aquosa contendo 0,01 mol de nitrato de chumbo II adiciona-se um volume pequeno de solução aquosa contendo 0,00002 mol de cromato de potássio, a quantidade máxima de precipitado de cromato de chumbo II que se forma é, em miligramas, aproximadamente igual a
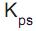 = 1,8 x 10-14 .
= 1,8 x 10-14 .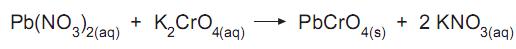
Se a uma solução aquosa contendo 0,01 mol de nitrato de chumbo II adiciona-se um volume pequeno de solução aquosa contendo 0,00002 mol de cromato de potássio, a quantidade máxima de precipitado de cromato de chumbo II que se forma é, em miligramas, aproximadamente igual a
Ano: 2011
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2011 - Transpetro - Técnico Químico |
Q170996
Química
O método Volhard, usado para determinar o ponto final em argentometria, é baseado na formação do íon complexo vermelho [(Fe(SCN)] 2+ quando excesso de Ag +é titulado com solução aquosa padrão de KSCN (ver etapas abaixo).
Etapa I - Adição de quantidade conhecida de Ag+ para garantir a reação completa com todo íon haleto (X- ) e excesso de Ag+ na solução Ag+(aq) + X- (aq) → AgX(s)
Etapa II - Titulação do excesso de Ag+
Ag+ (aq) + SCN-(aq) → AgSCN(s)
Etapa III - Formação de complexo vermelho com o primeiro excesso de SCN-
SCN- + Fe3+→ [(Fe(SCN)] 2+(aq)
Com base nas informações relativas a cada etapa do processo, analise as afirmações a seguir.
I - O SCN- atua como indicador do ponto ? nal da titulação.
II - Pelo fato de o valor do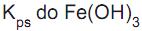 do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido.
do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido.
III - O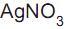 é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz.
é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz.
IV - Nas titulações argentométricas, os sais de prata tipo AgX são bem solúveis em água.
É correto APENAS o que se afirma em
Etapa I - Adição de quantidade conhecida de Ag+ para garantir a reação completa com todo íon haleto (X- ) e excesso de Ag+ na solução Ag+(aq) + X- (aq) → AgX(s)
Etapa II - Titulação do excesso de Ag+
Ag+ (aq) + SCN-(aq) → AgSCN(s)
Etapa III - Formação de complexo vermelho com o primeiro excesso de SCN-
SCN- + Fe3+→ [(Fe(SCN)] 2+(aq)
Com base nas informações relativas a cada etapa do processo, analise as afirmações a seguir.
I - O SCN- atua como indicador do ponto ? nal da titulação.
II - Pelo fato de o valor do
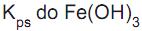 do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido.
do Fe(OH) 3 ser 4 x 10-38 , o método de Volhard só funciona se o pH da solução for muito ácido. III - O
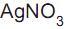 é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz.
é um padrão primário, pois sofre alteração fotoquímica quando exposto à luz. IV - Nas titulações argentométricas, os sais de prata tipo AgX são bem solúveis em água.
É correto APENAS o que se afirma em