Questões de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess. para Concurso
Foram encontradas 358 questões
Ano: 2023
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2023 - Transpetro - Técnico de Dutos |
Q2319824
Química
Um balão flexível contém um gás que se comporta idealmente. Na situação inicial, o volume ocupado pelo gás é
de 35,0 m3
a 25,0°C e 1,00 atm. Considere o aquecimento do balão, com expansão do volume para 50,0 m3
, de
tal forma que a pressão permaneceu constante.
Nessa situação final, a temperatura do balão, em K, é
Dado T(K) = T(°C) + 273
Nessa situação final, a temperatura do balão, em K, é
Dado T(K) = T(°C) + 273
Q2297501
Química
A figura 2 mostra o diagrama de fases do sistema água - cloreto de sódio, concentração por massa em
pressão atmosférica.
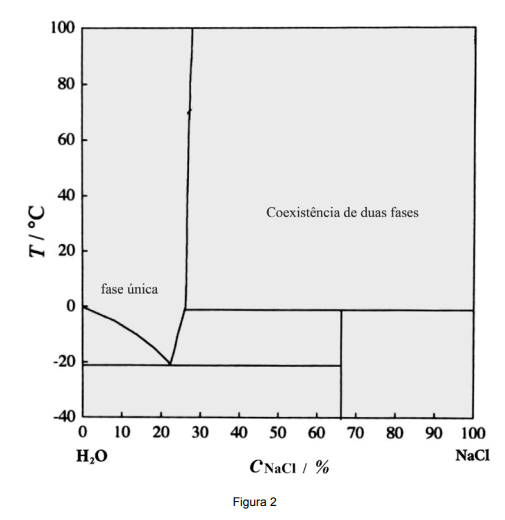
K. Endoh, H. Suga. Thermochimica Acta 327, 1999, p. 134. (Adaptado).
Assinale V (verdadeiro) ou F (falso) diante de cada afirmativa a seguir.
( ) Água com 22% de sal solidifica por volta de -21 ºC.
( ) Em 0 ºC, a água se solidifica para concentrações de sal maiores que 25%.
( ) O gelo flutuando no oceano contém sal de acordo com a linha de liquidus.
( ) A concentração máxima de sal dissolvido em água é de 26% em 20 ºC.
Assinale a alternativa com a sequência correta.

K. Endoh, H. Suga. Thermochimica Acta 327, 1999, p. 134. (Adaptado).
Assinale V (verdadeiro) ou F (falso) diante de cada afirmativa a seguir.
( ) Água com 22% de sal solidifica por volta de -21 ºC.
( ) Em 0 ºC, a água se solidifica para concentrações de sal maiores que 25%.
( ) O gelo flutuando no oceano contém sal de acordo com a linha de liquidus.
( ) A concentração máxima de sal dissolvido em água é de 26% em 20 ºC.
Assinale a alternativa com a sequência correta.
Ano: 2023
Banca:
FGV
Órgão:
SEE-MG
Prova:
FGV - 2023 - SEE-MG - Professor de Educação Básica (PEB) - Química |
Q2289236
Química
Os parâmetros termodinâmicos de uma reação química são de
fundamental importância para a compreensão de seu
processamento. A tabela a seguir apresenta os valores de
variação de entalpia (ΔH), variação de entropia (ΔS) e
temperatura para quatro processos distintos (I, II, III e IV)
realizados à pressão e temperatura constantes.
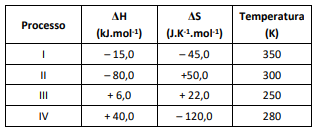
O processo espontâneo é o

O processo espontâneo é o
Ano: 2023
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
UFSJ
Prova:
FUNDEP (Gestão de Concursos) - 2023 - UFSJ - Técnico de Laboratório - Área: Química |
Q2285404
Química
O equipamento principal na soldagem oxiacetilênica é
o maçarico. Esse equipamento mistura o gás oxigênio
e o acetileno (C2
H2
) em proporções adequadas,
produzindo uma chama quente o suficiente para soldar
e cortar. Sabe-se que a ∆H0
de combustão completa
do acetileno libera 1556 kJ/mol. Considere que 63 mg
de água foi produzido no processo de combustão do
gás acetileno.
Qual o valor mais próximo, em quilojoules, da energia liberada nesse processo?
Qual o valor mais próximo, em quilojoules, da energia liberada nesse processo?
Ano: 2023
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
UFSJ
Prova:
FUNDEP (Gestão de Concursos) - 2023 - UFSJ - Técnico de Laboratório - Área: Química |
Q2285399
Química
O grafite e o diamante são formas cristalinas de um
único elemento químico. Ambos são feitos do mesmo
elemento, ou seja, são formas alotrópicas do carbono.
Apesar de serem compostos do mesmo elemento,
o diamante é o mineral mais duro conhecido pelo
homem e o grafite é um dos mais suaves. No entanto,
a combustão do grafite e do diamante apresenta valores
de variação da entalpia muito próximos. Considere as
equações químicas a seguir:
Cgrafite + O2 (g) → CO2 (g) ∆H = – 393,5 kJ mol–1
Cdiamante + O2 (g) → CO2 (g) ∆H = – 395,4 kJ mol–1
Qual a variação de entalpia necessária, em quilojoules para converter um mol de grafite em diamante?
Cgrafite + O2 (g) → CO2 (g) ∆H = – 393,5 kJ mol–1
Cdiamante + O2 (g) → CO2 (g) ∆H = – 395,4 kJ mol–1
Qual a variação de entalpia necessária, em quilojoules para converter um mol de grafite em diamante?