Questões Militares Comentadas sobre química para ibfc
Foram encontradas 27 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Adaptado. Disponível em: Petróleo: o que é e para que serve? - eCycle. Acesso: 06 de janeiro de 2022
Observe as imagens a seguir.

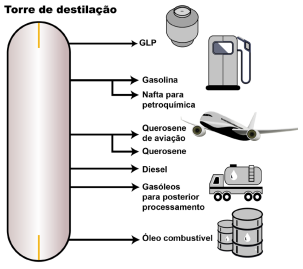
Imagem(Adaptado) . Torre de fracionamento do petróleo. Disponível em: https://combustivel-energia.blogspot.com/2012/10/ petroleo-e-derivados.html. Acesso: 06 de janeiro de 2022.
Utilizando os dados contidos na questão e seus conhecimentos sobre a obtenção de combustíveis a partir do petróleo, assinale a alternativa correta que apresenta o processo de separação de misturas mais relevante durante a obtenção destes combustíveis e a propriedade física adequada utilizada para esta separação, respectivamente.
Adaptado. Disponível em: Cobre: Ocorrência, obtenção industrial, propriedades e utilização - UOL Educação. Acesso: 05 de janeiro de 2022.
Um dos minérios mais utilizados na obtenção do cobre metálico é a calcosita, que pode ser representada pela fórmula Cu2 S. Um método de retirada do enxofre do minério é o processo de ustulação (por meio de aquecimento em presença de ar seco, rico em gás oxigênio). Observe a equação não balanceada a seguir, que representa o processo citado anteriormente:
Cu2S + O2 → Cu + SO2
Após o balanceamento da equação anterior, assinale a alternativa que apresenta qual é a massa aproximada (em gramas) de cobre metálico que pode ser obtida a partir de 2,0 Kg de Cu2S, com 60% de pureza e gás oxigênio suficiente. (Dados: massas atômicas - Cu = 63,5; S = 32).
Al0 + 3Ag+ → Al3+ + 3Ag0
A partir desta observação da pilha acima representada pela equação, assinale a alternativa correta.
C6H12O6(s) + 602(g) → 6CO2(g) + 6 H2O (l) ∆H0 combustão = – 2800 kj/mol
Considere os seguintes dados de massa molar em g/mol:
C=12, H=1, O=16
Com base nas informações do enunciado, assinale a alternativa que apresenta a energia obtida e a quantidade de CO2 liberada na oxidação de 18 g (gramas) de glicose.
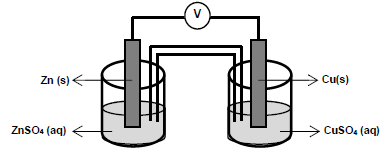
As semirreações que descrevem o processo de oxirredução estão descritas a seguir.
Cu2+ (aq) + 2e- → Cu(s) E0red = + 0,34 V (volts) Zn2+ (aq) + 2e- → Zn(s) E0red = - 0,76 V (volts)
Para o processo descrito, analise as afirmativas abaixo e dê valores Verdadeiro (V) ou Falso (F).
( ) O eletrodo de zinco sofre oxidação e o eletrodo de cobre sofre redução. ( ) A reação de oxidação ocorre no cátodo e reação de redução ocorre no ânodo. ( ) O diagrama de célula do processo é Zn (s)|Zn2+(aq)||Cu2+(aq)|Cu (s). ( ) Os elétrons fluem do ânodo para o cátodo. ( ) A reação global da pilha é Cu(s) + Zn2+(aq) → Cu2+(aq) + Zn(s) e a diferença de potencial é 1,10 V (volts).
Assinale a alternativa que apresenta a sequência correta de cima para baixo.