Questões da Prova CESGRANRIO - 2012 - Transpetro - Químico de Petróleo Júnior
Foram encontradas 2 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2012 - Transpetro - Químico de Petróleo Júnior |
Q258127
Química
A figura ilustra a eletrodeposição, processo inverso ao da pilha. É um dos mais importantes métodos de revestimento aplicados a materiais para protegê-los da corrosão.
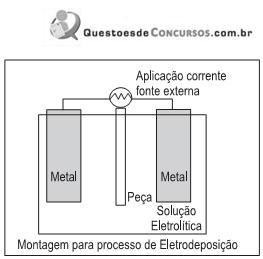
Esse processo consiste na aplicação de células eletrolíticas que utilizam energia elétrica para produzir reações de oxirredução não espontâneas, além de permitir o(a)

Esse processo consiste na aplicação de células eletrolíticas que utilizam energia elétrica para produzir reações de oxirredução não espontâneas, além de permitir o(a)
Ano: 2012
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2012 - Transpetro - Químico de Petróleo Júnior |
Q258101
Química
Não há metal que possa ser usado em todas as aplicações, pois todos os metais ou ligas podem sofrer os fenômenos de degradação pela corrosão. No caso das refinarias de petróleo, por exemplo, processos de corrosão do ferro podem ser ocasionados pela ação corrosiva do ar atmosférico. Abaixo estão representadas as equações químicas gerais não balanceadas da formação da ferrugem, seja na forma de Fe2 O3 ou Fe3 O4 .
Fe (s) + O2 + H2 O (vapor) → Fe(OH)2 Fe(OH)2 + O2 (g) → Fe2 O3 H2 O (vermelha ou castanha) + H2 O
Fe(OH)2 → Fe3 O4 (preto)+H2 O +H2 Nas reações descritas pelas equações acima, observa-se que o ferro
Fe (s) + O2 + H2 O (vapor) → Fe(OH)2 Fe(OH)2 + O2 (g) → Fe2 O3 H2 O (vermelha ou castanha) + H2 O
Fe(OH)2 → Fe3 O4 (preto)+H2 O +H2 Nas reações descritas pelas equações acima, observa-se que o ferro