Questões de Concurso Sobre sistemas homogêneos: constantes: kc e kp. deslocamento do equilíbrio: fatores. em química
Foram encontradas 242 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Um exemplo clássico de uma reação química em
equilíbrio é a reação entre o monóxido de
nitrogênio (NO) e o dióxido de nitrogênio (NO): 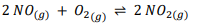
Nesta reação, o monóxido de nitrogênio (NO) reage com o oxigênio (O2) para formar dióxido de nitrogênio (NO2), e também ocorre a reação reversa, na qual o dióxido de nitrogênio (NO2) se decompõe para formar monóxido de nitrogênio (NO) e oxigênio (O2).
Assinale a alternativa que contém a equação para a constante de equilíbrio (KC) para esta reação.
Considerando a equação de equilíbrio a 160 °C
PCl5(g) ←→ PCl3(g) + Cl2(g)
Foi realizado um experimento, à mesma temperatura, e após o equilíbrio determinaram-se as seguintes concentrações:
[PCl5] = 0,027 mol.L-1
[PCl3] = 0,046 mol.L-1
[Cl2] = 0,012 mol.L-1
Desse modo, pode-se dizer que o valor da constante Kc corresponde, aproximadamente, a:
As pressões parciais iniciais de nitrogênio e hidrogênio em um vaso rígido selado são 0,020 e 0,030 bar, respectivamente. A mistura é aquecida até uma temperatura em que Kp = 0,11 para N2(g) + 3H2(g) ⇌ 2NH3(g)
Com base nisso, quais são as pressões parciais de cada substância na mistura de reação no equilíbrio?
Dada a seguinte reação, que se encontra em equilíbrio e ocorre em uma solução não saturada dos componentes, marque a opção correta.
2Fe3+ + 2S2O32− ⇌ 2Fe2++S4O62−
Com referência aos conceitos de equilíbrio químico, julgue o item.
Quando um sistema atinge o equilíbrio químico, as reações químicas se cessam.