Questões de Concurso Público IF-RS 2018 para Técnico de Laboratório - Química
Foram encontradas 3 questões
Ano: 2018
Banca:
IF-RS
Órgão:
IF-RS
Prova:
IF-RS - 2018 - IF-RS - Técnico de Laboratório - Química |
Q923313
Química
A reação do fósforo branco com ácido
nítrico e água gera como produtos ácido
fosfórico e óxido nítrico, conforme a reação de
oxirredução abaixo.
___ P + ___ HNO3 + __ H2O →__ H3PO4 + 5 NO
Após balanceamento, a soma dos coeficientes estequiométricos dos reagentes é __________. Nesta reação, o __________sofre oxidação e o __________sofre redução.
Assinale a alternativa que apresenta as palavras que preenchem CORRETAMENTE as lacunas, na ordem em que aparecem no texto:
___ P + ___ HNO3 + __ H2O →__ H3PO4 + 5 NO
Após balanceamento, a soma dos coeficientes estequiométricos dos reagentes é __________. Nesta reação, o __________sofre oxidação e o __________sofre redução.
Assinale a alternativa que apresenta as palavras que preenchem CORRETAMENTE as lacunas, na ordem em que aparecem no texto:
Ano: 2018
Banca:
IF-RS
Órgão:
IF-RS
Prova:
IF-RS - 2018 - IF-RS - Técnico de Laboratório - Química |
Q923314
Química
Dadas as seguintes semi-reações:
Fe+2(aq) + 2 e- → Fe(s) E° = - 0,44 V Pb+2(aq) + 2 e- → Pb(s) E°= - 0,13 V
E considerando a formação de uma pilha, são feitas as seguintes afirmativas:
I. A reação que ocorre no cátodo é Pb+2(aq) + 2 e- → Pb(s). II. A Pilha pode ser representada por Fe2+(aq) / Fe(s) // Pb2+(aq) / Pb(s). III. A voltagem da pilha é igual a 0,31 V. IV. A reação não é espontânea.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
Fe+2(aq) + 2 e- → Fe(s) E° = - 0,44 V Pb+2(aq) + 2 e- → Pb(s) E°= - 0,13 V
E considerando a formação de uma pilha, são feitas as seguintes afirmativas:
I. A reação que ocorre no cátodo é Pb+2(aq) + 2 e- → Pb(s). II. A Pilha pode ser representada por Fe2+(aq) / Fe(s) // Pb2+(aq) / Pb(s). III. A voltagem da pilha é igual a 0,31 V. IV. A reação não é espontânea.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
Ano: 2018
Banca:
IF-RS
Órgão:
IF-RS
Prova:
IF-RS - 2018 - IF-RS - Técnico de Laboratório - Química |
Q923330
Química
Soluções de peróxido de hidrogênio são
normalmente empregadas para fins estéticos.
Sua concentração é expressa em volumes e
comercialmente recebe o nome de “água
oxigenada”. A determinação da concentração do
peróxido nesta solução pode ser realizada por
permanganometria (reação 1). Este valor pode ser
expresso em “volumes”, conforme rótulos do
produto comercial, podendo ser calculado de
acordo com reação 2 .
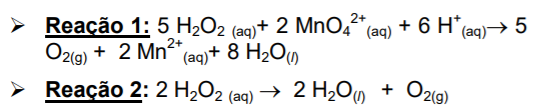
Com relação às informações dadas, podemos afirmar que:
I. A determinação de peróxido é um método complexiométrico. II. A expressão da concentração, em volumes decorre da auto protólise do peróxido. III. Na reação de permanganometria, o peróxido de hidrogênio é o agente redutor. IV. Para este procedimento deve ser empregado um indicador metalocrômico. V. A expressão “volumes de água oxigenada” se deve à geração de oxigênio na sua decomposição.
Estão CORRETAS apenas as afirmativas:
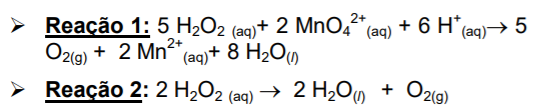
Com relação às informações dadas, podemos afirmar que:
I. A determinação de peróxido é um método complexiométrico. II. A expressão da concentração, em volumes decorre da auto protólise do peróxido. III. Na reação de permanganometria, o peróxido de hidrogênio é o agente redutor. IV. Para este procedimento deve ser empregado um indicador metalocrômico. V. A expressão “volumes de água oxigenada” se deve à geração de oxigênio na sua decomposição.
Estão CORRETAS apenas as afirmativas: