Questões de Concurso Público COMPESA 2018 para Analista de Saneamento - Engenheiro Químico
Foram encontradas 5 questões
Ano: 2018
Banca:
FGV
Órgão:
COMPESA
Prova:
FGV - 2018 - COMPESA - Analista de Saneamento - Engenheiro Químico |
Q919458
Química
A massa de hidróxido de sódio contida em 100 mL de uma
solução de pH 9 a 25°C é:
Dados: massas molares em g.mol-1 : H = 1; O = 16; Na = 23.
Dados: massas molares em g.mol-1 : H = 1; O = 16; Na = 23.
Ano: 2018
Banca:
FGV
Órgão:
COMPESA
Prova:
FGV - 2018 - COMPESA - Analista de Saneamento - Engenheiro Químico |
Q919465
Química
Na utilização de carbonato de sódio como padrão primário foi
pesado 2,650 g de carbonato de sódio anidro PA, previamente
dessecado a 200 °C durante uma hora. Esse sólido foi dissolvido,
num béquer, com água deionizada e transferido para um balão
de 500 mL completando assim esse volume. 10 mL dessa solução
de carbonato de sódio serão utilizados, numa titulação, para
padronizar uma solução 0,1 mol.L-1 de ácido clorídrico com
alaranjado de metila como indicador.
O volume previsto de titulado que deverá ser gasto nesse processo, considerando nenhum tipo de perda será de
Dados: massas molares (g.mol-1) C= 12; O=16; Na= 23.
O volume previsto de titulado que deverá ser gasto nesse processo, considerando nenhum tipo de perda será de
Dados: massas molares (g.mol-1) C= 12; O=16; Na= 23.
Ano: 2018
Banca:
FGV
Órgão:
COMPESA
Prova:
FGV - 2018 - COMPESA - Analista de Saneamento - Engenheiro Químico |
Q919467
Química
O esgoto doméstico é uma das principais fontes de poluentes
orgânicos despejados nos corpos d’água.
Se a quantidade de matéria orgânica e de microrganismos aeróbios no esgoto for alta, a diminuição da concentração de oxigênio dissolvido no meio provocará alterações no ambiente aquático.
A quantidade de oxigênio necessária para o consumo da matéria orgânica pode ser avaliada em laboratório, utilizando o excesso do reagente
Se a quantidade de matéria orgânica e de microrganismos aeróbios no esgoto for alta, a diminuição da concentração de oxigênio dissolvido no meio provocará alterações no ambiente aquático.
A quantidade de oxigênio necessária para o consumo da matéria orgânica pode ser avaliada em laboratório, utilizando o excesso do reagente
Ano: 2018
Banca:
FGV
Órgão:
COMPESA
Prova:
FGV - 2018 - COMPESA - Analista de Saneamento - Engenheiro Químico |
Q919469
Química
A alcalinidade total de uma amostra de 40,00mL da água de um
reservatório foi determinada por titulação utilizando ácido
clorídrico 0,0020 mol.L-1 previamente padronizado. No
procedimento de análise, 3 gotas de solução de fenolftaleína 1%
foram adicionadas a amostra que permaneceu incolor; em
seguida, foram adicionadas 3 gotas de solução de alaranjado de
metila 0,2% e a amostra foi titulada consumindo 7,50 mL do
ácido clorídrico.
A alcalinidade total da amostra, em mgCaCO3.L-1, corresponde aproximadamente a
Dados: massas molares em g.mol-1: C = 12; O = 16; Ca = 40. Equação para a titulação: 2HCl + CaCO3 → CaCl2 + H2O + CO2.
A alcalinidade total da amostra, em mgCaCO3.L-1, corresponde aproximadamente a
Dados: massas molares em g.mol-1: C = 12; O = 16; Ca = 40. Equação para a titulação: 2HCl + CaCO3 → CaCl2 + H2O + CO2.
Ano: 2018
Banca:
FGV
Órgão:
COMPESA
Prova:
FGV - 2018 - COMPESA - Analista de Saneamento - Engenheiro Químico |
Q919470
Química
O gráfico a seguir apresenta a curva de calibração para a
determinação da concentração de fósforo reativo em amostras
de águas doces utilizando o método do ácido ascórbico.
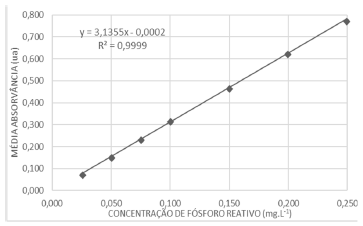
Nas mesmas condições analíticas uma amostra de água doce de um reservatório classe 2 com concentração desconhecida apresentou absorvância média 0,142 ua.
A concentração de fósforo reativo (em mg.L-1) na amostra é, aproximadamente, de

Nas mesmas condições analíticas uma amostra de água doce de um reservatório classe 2 com concentração desconhecida apresentou absorvância média 0,142 ua.
A concentração de fósforo reativo (em mg.L-1) na amostra é, aproximadamente, de