Questões de Concurso Público FIOCRUZ 2010 para Tecnologista em Saúde - Flexografia
Foram encontradas 16 questões
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Provas:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Produção de Vacinas Virais
|
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q567549
Farmácia
Em consonância com as BPF (Resolução da ANVISA, RDC
17 DE 2010), a empresa deve identificar quais os trabalhos
de qualificação e validação são necessários para comprovar
que todos os aspectos críticos de operação estejam sob
controle. A qualificação e a validação devem estabelecer e
fornecer evidências documentadas dos seguintes itens,
exceto,:
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568612
Farmácia
A Resolução - RDC N° 17, de 16 de abril de 2010 “Dispõe
sobre as Boas Práticas de Fabricação de Medicamentos",
preceitua que o gerenciamento da qualidade determina a
implementação da "Política da Qualidade", ou seja, as
intenções e as diretrizes globais relativas à qualidade,
formalmente expressa e autorizada pela administração
superior da empresa. Os elementos básicos do
gerenciamento da qualidade devem ser:
I. infra-estrutura apropriada ou "sistema de qualidade", englobando instalações, procedimentos, processos e recursos organizacionais.
II. ações sistemáticas necessárias para assegurar com confiança adequada que um produto (ou serviço) cumpre seus requisitos de qualidade. A totalidade dessas ações é chamada de "garantia da qualidade".
III. fundamentos e diretrizes da norma NBR ISO 9001:2000 que estabelece os requisitos mínimos para implantação do Sistema de Gestão da Qualidade.
Assinale:
I. infra-estrutura apropriada ou "sistema de qualidade", englobando instalações, procedimentos, processos e recursos organizacionais.
II. ações sistemáticas necessárias para assegurar com confiança adequada que um produto (ou serviço) cumpre seus requisitos de qualidade. A totalidade dessas ações é chamada de "garantia da qualidade".
III. fundamentos e diretrizes da norma NBR ISO 9001:2000 que estabelece os requisitos mínimos para implantação do Sistema de Gestão da Qualidade.
Assinale:
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568614
Farmácia
De acordo com a Resolução – RDC N° 17, de 16 de abril de
2010, os processos e procedimentos devem ser submetidos
à revalidação para garantir que se mantenham capazes de
atingir os resultados esperados. Existem 2 tipos de
revalidação: Revalidação Periódica e Revalidação após
Mudanças. Quando uma revalidação periódica for realizada,
os seguintes documentos devem ser considerados:
I. fórmula mestra e especificações.
II. procedimentos operacionais.
III. registros (ex., registros de calibração, manutenção e limpeza).
IV. métodos analíticos.
Assinale
I. fórmula mestra e especificações.
II. procedimentos operacionais.
III. registros (ex., registros de calibração, manutenção e limpeza).
IV. métodos analíticos.
Assinale
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568615
Farmácia
A Resolução - RDC N° 17, de 16 de abril de 2010 que
“Dispõe sobre as Boas Práticas de Fabricação de
Medicamentos", determina que qualificação e a validação
devem estabelecer e fornecer evidências documentadas de
que:
I. instalações, utilidades, sistemas computadorizados, equipamentos e processos foram projetados em consonância com as exigências de BPF (qualificação de projeto ou QP).
II. instalações, utilidades, sistemas computadorizados e equipamentos foram construídos e instalados de acordo com as suas especificações de projeto (qualificação de instalação ou QI).
III. instalações, utilidades, sistemas computadorizados e equipamentos operam de acordo com suas especificações planejadas (qualificação de operação ou QO).
IV. uma metodologia analítica e um processo específico produzirá um produto que consistentemente atenda suas especificações e atributos de qualidade (validação de processo ou VP, também chamada em alguns casos de qualificação de desempenho ou QD).
Assinale:
I. instalações, utilidades, sistemas computadorizados, equipamentos e processos foram projetados em consonância com as exigências de BPF (qualificação de projeto ou QP).
II. instalações, utilidades, sistemas computadorizados e equipamentos foram construídos e instalados de acordo com as suas especificações de projeto (qualificação de instalação ou QI).
III. instalações, utilidades, sistemas computadorizados e equipamentos operam de acordo com suas especificações planejadas (qualificação de operação ou QO).
IV. uma metodologia analítica e um processo específico produzirá um produto que consistentemente atenda suas especificações e atributos de qualidade (validação de processo ou VP, também chamada em alguns casos de qualificação de desempenho ou QD).
Assinale:
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568616
Farmácia
De acordo a Resolução - RDC N° 17, de 16 de abril de 2010
pode-se definir validação como o ato documentado que
atesta que qualquer procedimento, processo, equipamento,
material, atividade ou sistema realmente e consistentemente
leva aos resultados esperados. Ainda, em consonância com
essa mesma norma, existem diferentes tipos e abordagens
com relação à validação. Relacione a coluna da esquerda
(tipos e abordagem) com a coluna da direita (definição) e
estabeleça a correta correspondência
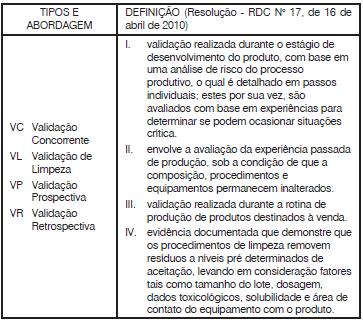
Estão corretas as associações

Estão corretas as associações